导语:
近日,苏州工业园区科技领军人才企业信达生物制药(苏州)有限公司传来捷报。公司创新药物PD-1抑制剂达伯舒(信迪利单抗注射液)获得中国国家药品监督管理局(NMPA)批准,联合含氟尿嘧啶类和铂类药物化疗用于不可切除的局部晚期、复发或转移性胃及胃食管交界处腺癌的一线治疗。这是首个获批胃癌适应证的国产抗PD-1单抗药物。至此,达伯舒也成为唯一在五大中国高发瘤种(肝癌、非鳞状非小细胞肺癌、鳞状非小细胞肺癌、食管癌、胃癌)一线治疗均获批适应证的PD-1抑制剂。
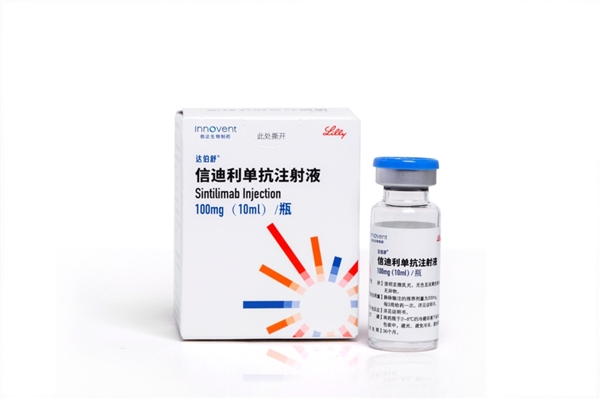
达伯舒是由信达生物和美国礼来共同开发、具有国际品质的国产PD-1单抗,于2018年12月在中国获批治疗复发/难治性经典型霍奇金淋巴瘤,2019年11月成为首个进入国家医保目录的PD-1单抗。截至目前,达伯舒共获批6项适应证,惠及上百万中国癌症患者。去年12月,达伯舒的三大一线适应证(非鳞状非小细胞肺癌、鳞状非小细胞肺癌、肝癌)纳入国家医保目录,成为中国医保内拥有最多一线适应证的PD-1产品。
信达生物制药集团总裁刘勇军表示,对于达伯舒今年新获批的食管癌和胃癌两项适应证,信达生物将积极参加国家医保谈判,希望早日纳入国家医保,提高患者用药可及性,继续践行“开发出老百姓用得起的高质量生物药”这一使命,让更多老百姓享受科技进步带来的健康成果,不断助力国家“健康中国2030”目标的早日实现。

“始于信,达于行”,开发出老百姓用得起的高质量生物药,是信达生物的理想和目标。信达生物成立于2011年,总部位于园区,2018年10月在港交所主板上市。公司入选2020年国家企业技术中心认定名单,同时也是江苏省唯一获批的创新型生物药企业。创立至今,公司形成了一条包括32个新药品种的产品链,覆盖肿瘤、代谢、免疫等多个疾病领域。其中7个产品入选国家“重大新药创制”专项,7个产品――达伯舒、达攸同、苏立信、达伯华、达伯坦、耐立克、希冉择已获批上市,3个新药分子进入III期或关键性临床研究,另外还有19个产品已进入临床研究。

经过“十余年如一日”的精耕细作,园区重点打造、面向未来的“一号产业”已在全国乃至全世界“出圈”。2021年实现产值1177亿元,产业产值连续多年保持20%以上增长,在最新的中国生物医药产业园区竞争力排名中,综合竞争力位居全国第一,五个单项竞争力中,产业竞争力、人才竞争力、技术竞争力均位列第一。
热门文章
中国台湾地区宣布6月30日前关停3G服务,闲置频段将投入5G发展
2024/4/1 17:12:02弗若斯特沙利文:百度文心一言稳居国产大模型第一
2024/3/27 14:26:11网飞版《三体》今日开播:刘慈欣担任顾问
2024/3/21 20:00:21小米汽车SU7/Pro/Max正式发布并上市,21.59万元起
2024/3/29 10:40:35特斯拉大裁员殃及上海厂,电动车该泼冷水了
2024/4/16 14:37:02艾瑞观点 | AIGC技术在营销领域应用三大方向
2024/3/29 10:27:22

扫一扫,或长按识别二维码
关注艾瑞网官方微信公众号