导语:
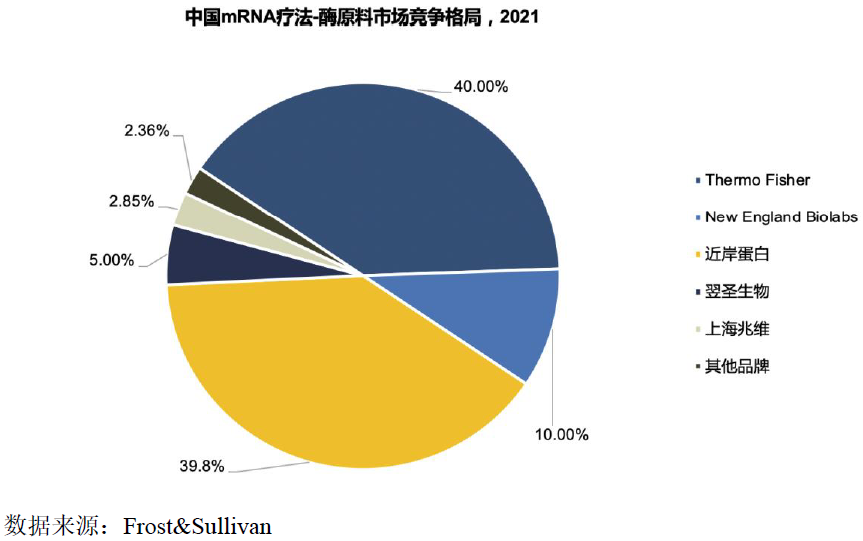
新冠爆发后,以BioNTech和Moderna为首率先上市的两款新冠mRNA疫苗为基础,掀起了国际上广泛的mRNA疫苗药物研究热潮。据Vision Research Peports 2022年8月份研究报告,全球mRNA疗法市场2021年达到了330亿美元规模。随后迅速在国内催生出mRNA疫苗原料酶赛道,根据Frost&Sullivan测算,原料成本是mRNA疗法生产成本的主要组成部分,约占生产总成本的58%。而酶原料大约占原料成本的39.58%,并预测2021年会达到52.2亿美元的全球市场规模。再看国内市场,由于mRNA疗法在传染病预防、肿瘤治疗、蛋白替代疗法等领域的多种应用场景,预计2025年,mRNA原料酶市场规模将达到14.7亿人民币。其中,苏州近岸蛋白质科技股份有限公司(以下简称“近岸蛋白”)mRNA原料酶在2021年度以39.8%的市场份额位居国内领先地位。在国内外众多酶原料供应商的竞争格局下,为什么近岸蛋白能够脱颖而出?
mRNA技术逐渐成熟
mRNA从被发现至今,已经过60余年的“锤炼”,以1990年为分水岭,mRNA技术实现了从机制研究到临床试验甚至产品上市的突破,技术路径逐渐成熟。其中关键技术突破有核苷酸单体修饰技术、mRNA递送技术,该两项技术是实现大规模人体临床试验开展的“核心动力”。随着技术的不断成熟和资本市场的助力,国内mRNA疗法也开启了快速发展之路。
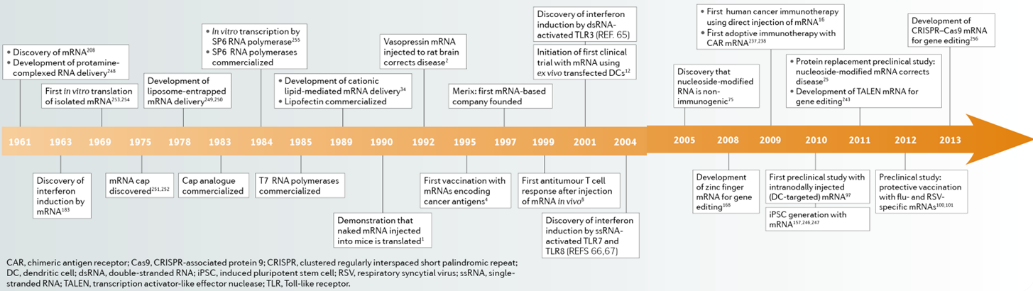
图片引自《mRNA-based therapeutics ―developing a new class of drugs》
新冠疫情引爆mRNA原料需求
在新冠mRNA疫苗投产之前,mRNA疫苗在全球范围都处于早研阶段,对原料的需求量小,因此国内外原料供应商的产能也是按照实验室或临床初期的需求进行设计安排。但是mRNA疫苗的成功研发和量产完全打破了这一局面,它对原材料的需求量是实验室阶段的成千上万倍,对原料的质量体系建设同时提出了更新更高的要求,致使整个产业链的上下游均受到了极大的冲击。辉瑞公司CEO阿尔伯特?布尔拉(Albert Bourla)曾警告,全球针对疫苗高度专业化的生产原料的争夺愈发激烈。他透露:“辉瑞的疫苗需要19个国家的86个供应商提供280种生产原料。”
专业的团队做专业的事
查看近岸蛋白的领导团队不难发现,大多为技术出身,且有生物药研发生产背景。董事长兼CEO朱化星博士,2005年获得复旦大学发育生物学博士学位,于1996年至2000年就职医药企业,具有丰富的药品研发及生产管理经验,因此更加知道药用原料的生产和质量管理至关重要。面对mRNA原料酶被应用到药物生产的需求,果断决策,布局建设GMP级原料酶生产基地。基地设计规模达到年产50亿人份mRNA疫苗原料酶,首期建设已完成2条2000L规模发酵、纯化和制剂的规模化生产线,部分品种单批次生产规模达千克级。在规划设计过程中,考虑到成本、长远供应及采购挤兑等问题,近岸蛋白在产能方面做了3至5倍的冗余,确保未来10年内原料的持续输出。产能之外,供应链问题的另一个维度是质量。mRNA疫苗属于一个全新的生产与质量控制体系,近岸蛋白在原料生产之初便把质控提高到药用级别,建立了严格的质量管理体系,并通过ISO9001、14001、45001等质量管理体系认证,形成上千页的技术文件、检测和管理文件,与原料一并移交给客户,以节约客户在原料放行等检测方法上的研发成本,更好地集中精力做核心研发。通过二十余家mRNA药物生产商的审计,获得客户高度认可。正是因为这些储备,使近岸蛋白mRNA原料酶成为国内唯一进入三期临床的品牌。
成功背后必然有苦行僧式的产品开发探索过程
从招股书获悉,近岸蛋白在mRNA原料领域布局多年,公司mRNA原料酶研发,始于以基因工程为基础,开发生产重组蛋白,应用于抗体药、mRNA疫苗药物、细胞与基因治疗等各个领域,在多年的客户积累后,与国内多家细胞治疗企业建立了深入的合作关系,并在2018年针对mRNA在肿瘤细胞治疗中的应用,完成了全套mRNA原料体系的开发。
据悉,在每个产品十余项的质量控制指标建立中,方法学的开发及质控标准的评定需要翻阅数百份参考文献及全球各地区药品原辅料质控标准文件,还需要做成百上千次的实验验证。在产品规模化生产前,需要做数千次的小试工艺和放大工艺可行性实验探索研究,同时需要做到严格控制工艺参数,在相对宽泛的工艺条件下确保产品的稳定性。
机会只垂青有准备的人
在全球mRNA疫苗药物开发黄金时期,国产mRNA疫苗要出海,必将面临各地区的政策法规要求。面对这一问题,近岸蛋白率先考虑到酶原料需要做出相应准备,于2021年将全套酶产品做了美国FDA DMF备案,使药物申报者可以直接使用DMF备案编号来代替申报过程中需要提供有关原料的具体信息,节约审批成本,提高审批效率。同时,面对部分有清真需求的地区,mRNA疫苗生产商需要保证其产品所有物料溯源达到清真要求,据悉,近岸蛋白于2022年将其mRNA原料生产基地菏泽工厂进行了清真认证,免除mRNA疫苗生产商的后顾之忧。事实证明,机会只垂青有准备的人,近岸蛋白经过多年的技术储备和果断及时的产能扩建决策,以及想客户之想的服务意识,让其抓住了这次mRNA市场机遇,在众多供应商中脱颖而出。
热门文章
中国台湾地区宣布6月30日前关停3G服务,闲置频段将投入5G发展
2024/4/1 17:12:02弗若斯特沙利文:百度文心一言稳居国产大模型第一
2024/3/27 14:26:11小米汽车SU7/Pro/Max正式发布并上市,21.59万元起
2024/3/29 10:40:35特斯拉大裁员殃及上海厂,电动车该泼冷水了
2024/4/16 14:37:02艾瑞观点 | AIGC技术在营销领域应用三大方向
2024/3/29 10:27:22外媒热议小米SU7定价:比特斯拉便宜 彰显品牌信心
2024/3/29 12:12:26

扫一扫,或长按识别二维码
关注艾瑞网官方微信公众号